Detta är fjärde delen i en serie på fyra som handlar om samtycke i forskning i allmänhet och samtycke i Trötthetsstudien i synnerhet. Länkar till tidigare inlägg i serien hittar du längst ner på sidan.
De tre första delarna i den här serien har handlat om samtycke i forskning med störst, fokus på frivillighet och sårbara personer i den så kallade Trötthetsstudien. I den här delen problematiserar jag ytterligare ett par saker som berör frivillighet i samtycke i den aktuella studien.
AI-genererad sammanfattning
I den sista delen fortsätter genomgången av problem gällande samtycke och frivillighet i Trötthetsstudien. Författaren kritiserar processen för att remittera patienter till studien, där samtycke ges först efter att remissen skickats från primärvårdsläkaren, vilket kan leda till att känslig information delas utan ordentligt samtycke. Författaren varnar också för att den automatiserade algoritmen som används för att identifiera lämpliga deltagare kan förstärka maktobalansen mellan läkare och patienter, vilket ytterligare kan påverka samtyckets frivillighet.
Ett sent samtycke
Vi har alltså tidigare i den här serien kunnat konstatera att Trötthetsstudiens forskare vet att de potentiella deltagarna är sårbara och i beroendeställning till vården. Vi har också sett att forskarna i sin etikprövningsansökan lyfter fram att det finns en risk att vissa personer kan känna sig pressade att delta. Ändå ger potentiella deltagare sitt samtycke först efter att primärvårdsläkaren skickar remissen till forskarna och remissen har bedömts av forskargruppen. Relationen till rekryteraren verkar lämnas helt utanför den etiska prövningen som gjorts.
Den här bilden ligger på studiens hemsida
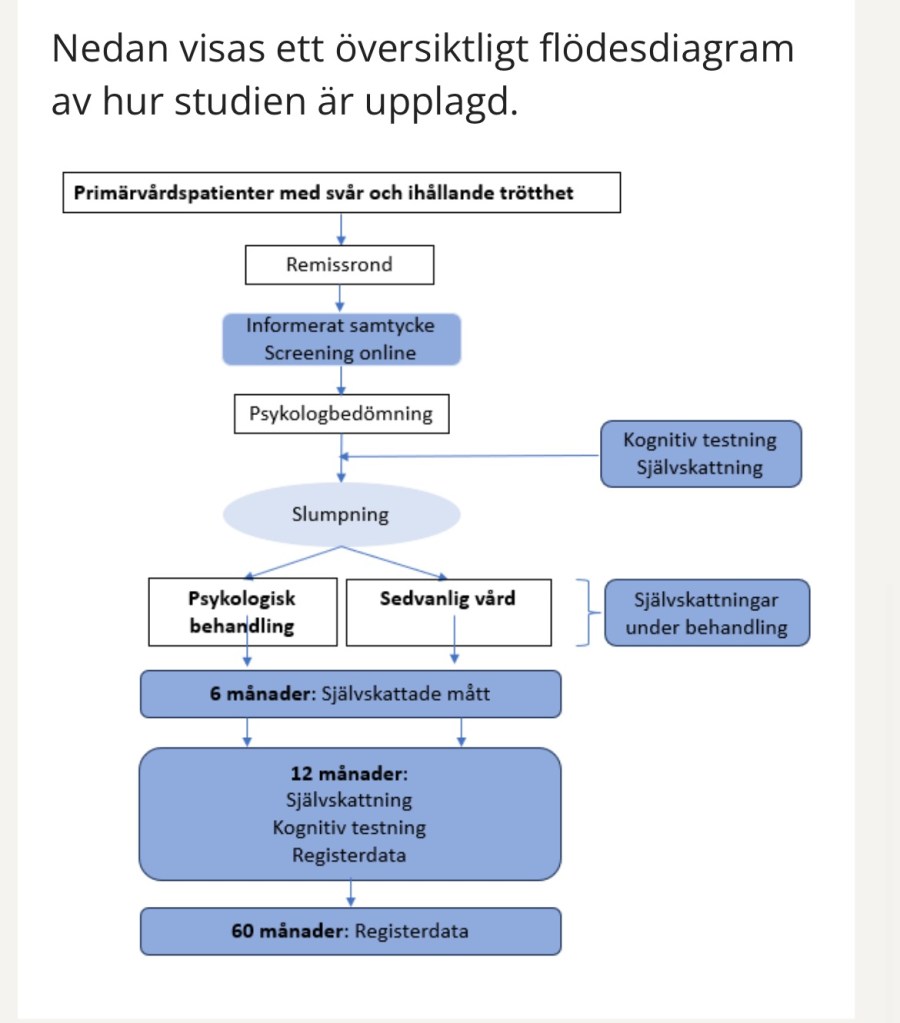
Skärmdump flödesschema
I etikprövningsansökan står följande:
”Deltagare remitteras till studien från sin husläkarmottagning (remiss till Gustavsbergs universitetsvårdcentral), utifrån en specificerad remissmall. Inkomna remisser granskas av projektgruppen (läkare, psykolog, forskningskoordinator) på veckobasis. I de fall då förtydliganden eller ytterligare provtagningar krävs skickas remissen tillbaka eller avslås. Om remissen godkänns kontaktas patienten via telefon och bokas för bedömningssamtal inför studien. Innan bedömningssamtalet ombeds patienten logga in på studiens forskningsplattform för att lämna informerat samtycke och fylla i screening som underlag för bedömningssamtalet (bakgrundsfrågor och självskattade symtomformulär).” (s.16)
Av etikprövningsansökan framgår att läkaren förväntas uppmuntra patienten att ta del av information som finns på studiehemsidan innan remissen skickas för bedömning.
”Potentiella studiedeltagare uppmuntras av sin läkare på vårdcentralen att läsa på hemsidan innan remiss till studien skickas. Om remissen godkänns kontaktas den potentiella studiedeltagaren av forskargruppen för att bokas till studiebedömning. Vid denna kontakt kan studiedeltagaren ställa frågor om studien och välja att tacka nej till fortsatt bedömning. Betänketid kan erbjudas vid behov. Om studiedeltagaren är intresserad av att gå vidare hänvisas till den digitala forskningsplattformen där all patientinformation är samlad och digitalt informerat samtycke kan lämnas (med BankID) innan påbörjad screening. Patientinformationen finns i utskriftsvänligt format på hemsidan och kan laddas ner på egen dator. Vid bedömningssamtalet ges ytterligare möjlighet att muntligt ge information om studien och stämma av att studiedeltagaren är införstådd i forskningsprojektet och fortsatt är intresserad av att delta.” (s. 19)
Men studiens hemsida saknar vad jag kan se information till läkaren om att hen förväntas uppmana potentiella deltagare att ta del av informationen på hemsidan.










Remissen skickas alltså som någon slags intresseanmälan som forskarna bedömer innan deltagaren tillfrågas om deltagande och ger formellt samtycke. Jag ser flera problem med detta förfarande.
Dels tänker jag att tillvägagångssättet i rekryteringen kan försvåra patienternas möjligheter att säga nej, eftersom läkaren genom remissen tagit ställning till att hen anser att patienten är en lämplig deltagare och lagt ner mycket arbete på att skriva remiss och att initiera eller genomföra utredningar specifikt inför studien. Och dels ser jag stora problem med att känslig information om patienten skickas till forskarna utan att det krävs formellt samtycke.
För att förklara problemen med detta behöver jag börja med att berätta vad som gäller för remisser inom vården.
Remittering och sekretess i vården
På grund av den starka sekretessen i vården krävs alltid en patients samtycke för att remiss ska kunna skickas mellan olika vårdgivare. Så här beskrivs det i vårdgivarguiden (som är en del av region Stockholms stöd till sina anställda inom vårdens verksamheter).
”Grundprincipen är att du som arbetar inom vården aldrig får lämna ut uppgifter utan patientens godkännande. Det gäller till exempel uppgifter om sjukdomar, behandling eller privat situation.”
”Tystnadsplikten gäller all personal inom vården. Oavsett om det är inom offentlig eller privat vård och oavsett om det är läkare, sjuksköterskor eller administrativ personal.”
”Också mellan personal hos en vårdgivare finns en skyldighet att respektera patientens integritet. Som huvudregel är det bara du som deltar i vården av en patient som får ta del av information om patientens hälsotillstånd eller personliga förhållanden.”
Så här beskrivs samtycket för remisser mellan vårdgivare i Vårdhandboken (som är ett metod- och kunskapsstöd för den som arbetar inom vården).
”När man som personal informerar en patient om kommande vårdåtgärder, till exempel en remiss, och patienten inte protesterar, förutsätts att patienten har gett sitt samtycke till att nödvändigt journalmaterial överförs med remissen. Detta är ett exempel på så kallat presumtivt samtycke.”
En läkare får alltså inte skicka en remiss till en annan vårdgivare utan att patienten vet om det. Då är det ett sekretessbrott. Men även om en remiss till Trötthetsstudien skulle skickas enligt vårdens regler gäller inte presumtivt samtycke i forskning.
Forskning kräver en annan typ av samtycke
Som jag beskrivit närmare i första inlägget i denna serie krävs en helt annan typ av samtycke. Forskaren kan aldrig anta att en deltagare samtycker, utan det krävs att forskaren har tagit reda på att samtycket är frivilligt, att forskningspersonen fått tillräckligt med information om studien och att samtycket m gäller en specifik studie. Samtycket ska vara uttryckligt och otvetydigt. Dessutom måste det dokumenteras och deltagaren ska få veta att det är möjligt att återta.
En forskare kan med andra ord aldrig förutsätta att en deltagare samtycker till något som inte är fullt uttalat på samma sätt någon i vården kan.
I ljuset av den här informationen undrar jag om inte samtycket i Trötthetsstudien ges för sent i processen? Att det mest rimliga vore att patienten fick lämna ett första samtycke innan remissen skickades för bedömning till forskargruppen.
Är remissen vård eller forskning?
När jag kollar igenom informationen på studiens hemsida framgår det dessutom att remissen ska skickas till Gustavsbergs vårdcentral som ”psykologkonsultation”.

Här verkar man alltså göra remitterandet till en del av vården trots att det i etikprövningsansökan och under rubriken remisshantering på hemsidan framgår att projektgruppen behandlar remissen vid en remissgenomgång inom ramen för studien.

Rutiner för rekrytering via remiss
För att förstå hur andra forskare gör med rekrytering via remiss har har jag gjort sökningar på nätet.
I informationen för en aktuell fas 1-studie på Akademiska sjukhuset om cancerbehandling framgår att läkaren måste prata med patienten om att remissen skickas och att detta ska dokumenteras:
”Patienten ska vara vidtalad när remissen skickas till oss. Det ska framgå i journalanteckningen eller remissen från er.”

Även vid likande verksamhet vid Karolinska sjukhuset understryker informationen att läkaren måste tala med patienten innan remissen ska skickas och att detta ska dokumenteras.

Jag hittar också information om en studie vid BUP i region Stockholm gällande internetförmedlad KBT vid OCD och där finns information om att det krävs samtycke från samtliga vårdnadshavare för att remiss ska kunna skrivas.

Hantering av känslig information
Utöver de frågetecken kring remittering och frivilligt samtycke som jag har tagit upp i det här avsnittet undrar jag vad som händer med de känsliga uppgifter läkaren skickar till forskarna i projektet via remissen. Vad jag kan se finns ingen information om hur dessa, eller de extra provtagningar och undersökningar som krävs för studien, ska hanteras varken i etikprövningsansökan eller på hemsidan – något som känns väldigt problematiskt.
Nu lämnar vi själva remissen och går vidare till ett annat problem.
Ett beslutsstöd som riskerar att öka maktövertaget
För att det ska bli enklare för läkaren att rekrytera patienter som forskarna anser vara lämpliga för studien har projektgruppen utvecklat ett automatiserat beslutsstöd som kopplats till region Stockholms journalsystem. Beslutsstödet består av en algoritm som söker av journalsystemet och uppmärksammar läkaren på lämpliga forskningsdeltagare när deras journal öppnas.
”Vår forskargrupp har utvecklat en algoritm i ALMA (ett helautomatiskt beslutsstöd kopplat till journalsystemet) för att stötta dig som läkare att identifiera patienter som lider av svår och ihållande trötthet. Algoritmen identifierar tidigare diagnoser och journalnotat som kan tyda på svår och ihållande trötthet. Om din husläkarmottagning är ansluten till ALMA kan du slå på detta beslutsstöd på din arbetsdator och få notiser från journalsystemet i samband med att du öppnar en patients journal. Observera att en klinisk bedömning alltid ska göras i varje enskilt ärende, och remiss till studien ska följa upprättad remissmall (se Remissbedömning och remissmall).”
Så här skriver bolaget bakom ALMA, som alltså är det system som forskarnas algoritm integrerats i:
”Medan läkaren koncentrerar sig på patienten, går ALMA igenom hela journalen – vid varje vårdbesök. Hon jämför den mot nationella och lokala rekommendationer, riktlinjer och kunskapsstöd. På så sätt hjälper hon läkaren att hitta avvikelser och kan förebygga risk för vårdskador. ALMA hjälper även till med administrationen genom att ta fram färdiga förslag på exempelvis remisser, provbeställningar och läkemedelsordinationer. ALMA stödjer idag över 200 olika riktlinjer inom 15 områden. Exempelvis KOL, diabetes, och hjärta kärl. Detta utökas löpande och all ny kunskap blir tillgänglig för alla som använder ALMA.”
Jag tänker att en sån här algoritm sannolikt ökar läkarens motivering att remittera patienter till projektet och att det är därför forskarna utvecklat den. Ska man hårddra det så påverkar alltså forskarna läkaren att påverka patienten – vilket högst sannolikt ökar läkarens maktövertag ytterligare.
Detta borde även öka risken att patientens samtycke inte är frivilligt. Och därmed ogiltigt.
Jag tänker också att det finns en risk att algoritmen gör att läkare som saknar kunskap, tid och behandlingsalternativ kan anse att det är motiverat att på olika sätt övertala en patient att delta i projektet.
Ett sådant här beslutsstöd behöver inte vara fel. Om det till exempel innehåller varningsflaggor relaterat till belastningsutlöst symtomförvärring (PEM) skulle det kunna hjälpa till att skydda dessa personer mot den KBT-behandling som studien erbjuder. Men med tanke på att bolaget skriver att ALMA uppdateras kontinuerligt med nya kunskapsstöd och riktlinjer tänker jag att det är sannolikt att Socialstyrelsens nationella kunskapsstöd för postinfektiösa sjukdomar redan har eller kommer att inkluderas i ALMA framöver.
Detta är djupt problematiskt med tanke på de risker som kunskapsstödet innebär för personer som lever med en sjukdom som ger PEM. Och eftersom Socialstyrelsens beslutsstöd driver samma pseudovetenskapliga linje och riskfyllda behandlingsrekommendationer gällande postinfektiösa sjukdomar som Trötthetsstudien kommer ett eventuellt inkluderande motverka ALMA:s syfte som alltså är att öka patientsäkerheten.
Det finns överhuvudtaget inga reflektioner kring eventuella risker med ett automatiserat beslutsstöd i etikprövningsansökan för Trötthetsstudien, inte heller några fördjupade exempel på vad det är forskarna i studien gett algoritmen i uppdrag att leta efter. Jag undrar också om det finns ett samband mellan utvecklandet av denna algoritm och de problematiska förändringar som gjordes i vårdprogrammet för ME i viss.nu under sommaren 2024, och där ansvarig forskare för Trötthetsstudien, Elin Lindsäter, stod som granskare.
Summering
Som jag ser det finns det stora etiska problem relaterat till försökspersonernas frivillighet i Trötthetsstudien och jag undrar hur den kunnat passera Etikprövningsmyndigheten utan krav på ändringar.
Jag skulle egentligen vilja fortsätta och prata mer om informationsdelen av samtycket i studien, men jag är inte riktigt färdigformulerad där ännu. För en viktig sak i det här med att vara informerad handlar om hur risker beskrivs och i etikprövningsansökan för studien är exempelvis PEM inte är upptaget som risk alls.
Men det handlar också om att den ansvariga forskaren Elin Lindsäter och flera andra i projektgruppen har kopplingar till lobbygruppen Oslo Chronic Fatigue Consortium och att deras ideologi tydligt påverkar synen på försökspersonerna. Detta framgår inte någonstans i informationen till deltagarna eller tas upp som intressekonflikt i etikprövningsansökan.
Jag hoppas att det här är något jag kan återkomma till längre fram.
Vill du läsa mer om Trötthetsstudien har jag samlat material på [denna sida]. Där hittar du bland annat ansökningar om medel, information om pilotprojekt och aktuell etikprövningsansökan.
Vill du lära dig mer om BPS-lobbyn, Oslo Chronic Fatigue Consortium och den ideologi de står för samt förstå det problematiska med Socialstyrelsens nationella kunskapsstöd rekommenderar jag [Maran säsong 2].
Länkar till inläggen i denna serie:
Del 4 (detta inlägg)
Uppföljande inlägg:
Nypublicerad artikel bekräftar etiska problem med Trötthetsstudien
Upptäck mer från The ME Inquiry Report
Prenumerera för att få de senaste inläggen skickade till din e-post.


Hej!
Du hav i vanlig ordning gjort en väldigt grundlig undersökning och analys!
Har du haft kontakt med ME-patienter som erbjudits deltagande i trötthetsstudien? Vilka erfarenheter har dom då haft i bemötandet? Om dom har tackat nej, har dom upplevt att dom fått ett annorlunda – sämre? – bemötande och vård efter detta? Och hur har dom patienter som tackat jag till deltagande i studien upplevt deltagandet? Det vore jätteintressant att veta!
GillaGillad av 1 person
Nej, jag har inte haft kontakt med någon som har blivit rekryterad till studien. Jag vet inte hur långt forskarna har kommit med rekryteringen, bara att sajten Clinical Trials uppger att man rekryterar. https://clinicaltrials.gov/study/NCT06786832?term=Lindsäter&rank=2
Däremot hade jag kontakt med en person som deltog i pilotstudien och du hittar hennes erfarenheter under rubriken pilotstudien på denna sida: https://mitteremitage.wordpress.com/trotthetsstudien/
GillaGillad av 1 person
Håller med Catrin!
Tycker mig återigen skönja den traditionella statusordningen med patienten nederst: respekterar man inte patienterna på ena sättet (genom att fråga dem först) så respekterar man dem inte heller på det andra (genom att lyssna på deras berättelser och då med utgångspunkten att de är tillräkneliga personer som kan bedöma sina egna erfarenheter; gör man sedan en annan bedömning ska man kunna redovisa goda skäl till det).
Illa nog när det gäller vårdpersonal; förödande i forskning.
GillaGillad av 1 person